第三幕:从游戏到基因——破解生命密码
在棋盘上证明了其学习算法的通用性和强大威力之后,DeepMind将目光投向了一个远比游戏复杂、且与人类福祉息息相关的领域:基础科学。Alpha血统的下一次进化,标志着其从抽象的符号世界向混乱而美妙的物理世界迈出的关键一步,目标直指一个困扰了生物学界半个世纪的“宏大挑战”。
1.下一个宏大挑战:蛋白质折叠问题
这个挑战就是蛋白质折叠问题(protein folding problem)。用通俗的语言来说,这个问题就是:如何仅根据蛋白质的一维氨基酸序列,预测出它在三维空间中折叠成的复杂、精确的立体结构?
这个问题之所以至关重要,是因为在生物学中,结构决定功能。蛋白质是生命活动的执行者,它们像微小的分子机器,催化化学反应、运输物质、构建细胞骨架。而一个蛋白质能执行何种功能,完全取决于它折叠成的独特三维形状。因此,能够准确预测蛋白质结构,就意味着能够解锁理解疾病机理、设计新药、乃至创造全新生物材料的钥匙。
然而,这个问题异常困难。一个典型的蛋白质由数百个氨基酸组成,其可能折叠的方式数量是一个天文数字。根据“莱文塔尔悖论”(Levinthal’s paradox),如果一个蛋白质要通过随机尝试所有可能的构象来找到其正确的折叠状态,所需的时间将比宇宙的年龄还要长。这使得通过暴力计算来解决问题变得不可能,其挑战的量级和性质,与围棋问题惊人地相似。这正是DeepMind选择它作为下一个目标的根本原因。
2.AlphaFold的胜利
2020年,在国际蛋白质结构预测竞赛(CASP)上,DeepMind的AlphaFold 2横空出世,其表现震惊了整个生物学界。它预测蛋白质结构的准确度,已经可以与耗时数月甚至数年、成本高昂的X射线晶体学等实验方法相媲美。这被广泛认为是生物学领域的一次革命性突破。
更具深远影响的是DeepMind接下来的决定。他们没有将这项强大的技术私藏,而是选择了一条开放科学的道路。他们利用AlphaFold 2预测了超过2亿种蛋白质的结构,几乎涵盖了所有已知科学的编目蛋白质,并将这些数据全部免费公开,创建了AlphaFold蛋白质结构数据库。
这一举动极大地推动了全球生命科学的研究进程。截至目前,该数据库已被来自190个国家的超过200万名研究人员使用,其原始论文的引用次数也已超过2万次。这无疑是AI赋能科学研究最光辉的范例之一。
3.开启生物学与医学的新纪元
AlphaFold的诞生,如同为生物学家们提供了一台“结构显微镜”,让他们能够以前所未有的速度和规模观察生命的微观世界。其现实世界的影响正在迅速显现:
- 加速药物研发:研究人员正在利用AlphaFold的预测来加速针对疟疾、帕金森病等疾病的药物研发。
- 对抗抗生素耐药性:通过理解细菌蛋白质的结构,科学家可以更好地设计药物来对抗日益严峻的抗生素耐药性问题。
- 解决环境问题:AlphaFold被用于设计能够更高效分解塑料垃圾的新型酶,为解决塑料污染问题提供了新的思路。
AlphaFold的角色并非取代人类科学家,而是成为他们强大的助手。它将科学家们从繁重、耗时的结构测定工作中解放出来,让他们能够将精力更多地投入到更高层次的、关于功能、机理和应用的创新性研究中。
4.分子生物学的未来:从预测到设计
Alpha血统的进化并未止步于预测。正如它在围棋领域从模仿人类(AlphaGo)进化到自我创造(AlphaGo Zero)一样,在生物学领域,它也正在实现从“分析”到“合成”的飞跃。
AlphaFold 3于2024年发布,标志着这一飞跃的开始。它不再仅仅预测单个蛋白质的结构,而是能够预测蛋白质、DNA、RNA以及小分子(通常是药物,被称为配体)之间复杂的相互作用网络。其核心架构也从AlphaFold 2的Evoformer模块,演进为一种基于
扩散模型(Diffusion model)的新架构。这种模型类似于AI图像生成器,从一团随机的原子“云”开始,逐步迭代,最终收敛到最精确的分子复合物结构。在预测这些关键的生物分子相互作用方面,AlphaFold 3的准确性比现有方法提高了至少50%。
AlphaFold 2 与 AlphaFold 3:分子生物学领域的代际飞跃
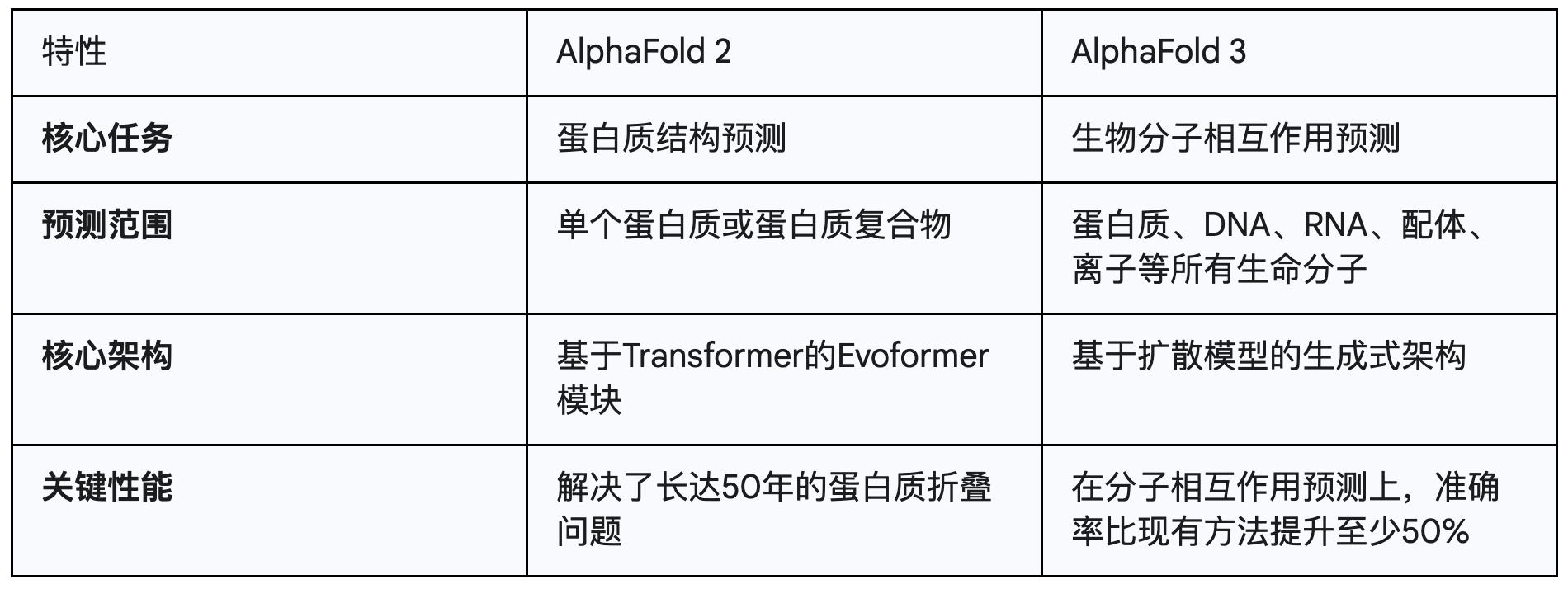
如果说AlphaFold 3让我们能“看见”生命之舞,那么AlphaProteo则让我们能“编排”这支舞蹈。AlphaProteo是DeepMind推出的一个用于从头设计(de novo design)全新蛋白质的AI系统。它不再是预测已知蛋白质的结构,而是根据给定的目标,创造出自然界中可能不存在的、能够特异性结合该目标的全新蛋白质——“结合蛋白”(binders)。
这在药物发现领域具有革命性潜力。例如,AlphaProteo已成功设计出能与癌症相关蛋白VEGF-A以及新冠病毒(SARS-CoV-2)刺突蛋白结合的全新蛋白质,其在湿实验室中的成功率和结合亲和力远超传统方法。这意味着AI正从一个理解生物学的工具,转变为一个工程化生物学的工具。这种从分析到合成的转变,预示着一个由AI驱动的、可编程的生物学新时代的到来,其在医药、材料科学和农业等领域的应用前景不可限量。
5. 破译指令手册:AlphaGenome
如果说AlphaFold系列让我们能够理解蛋白质这部“生命机器”的构造图,那么2025年6月发布的AlphaGenome则更进一步,旨在破译制造这些机器的终极“指令手册”——基因组 。这一进展标志着Alpha家族的探索深入到了生命科学最核心的领域:基因调控。
人类基因组计划完成后,科学家们发现了一个令人困惑的事实:只有不到2%的DNA序列直接编码蛋白质。那么,其余98%的“非编码DNA”(曾被误称为“垃圾DNA”)究竟是做什么的? 。现在我们知道,这片广阔的遗传“暗物质”是基因调控的中枢,它决定了在何时、何地、以何种强度开启或关闭特定的基因,而大多数与复杂疾病相关的遗传变异都发生在这个区域 。
AlphaGenome正是为了应对这一挑战而生。它是一个统一的DNA序列模型,旨在全面而准确地预测人类DNA序列中的单个突变(变异)如何影响调控基因的各种生物过程 。其核心突破在于解决了该领域长期存在的一个关键权衡:
- 长距离与高精度兼得:基因调控往往涉及远距离的相互作用,一个基因的开关可能位于数十万个DNA碱基之外。同时,一个单碱基的突变就可能产生深远影响。以往的模型要么只能分析短序列以保持高分辨率,要么只能分析长序列但牺牲精度 。AlphaGenome通过创新的架构,首次实现了同时分析长达100万个DNA碱基对的序列,并能以单个碱基的分辨率进行预测 。
- 统一的多模态预测:AlphaGenome不再是针对单一任务的“专家”,而是一个“通才”。它能够在一个统一的框架内,同时预测基因表达、RNA剪接、染色质可及性(DNA的开放程度)和蛋白质结合等多种分子特性 。在26项不同的变异效应预测基准测试中,AlphaGenome在24项上达到或超过了现有的顶尖专用模型 。
AlphaGenome的工作方式,是利用其强大的预测能力,对比正常DNA序列和发生突变的序列,从而快速(在GPU上不到一秒)评估一个变异可能带来的功能性影响 。例如,研究人员已经利用它成功地重现了一种已知的白血病致病机制:一个非编码区的突变如何错误地激活了一个本应沉默的致癌基因 。
通过向非商业研究领域开放API,AlphaGenome为全球科学家提供了一个强大的“数字显微镜”,使他们能够以前所未有的规模和速度筛选遗传变异,形成关于疾病机理的假设,并最终加速新疗法和药物靶点的发现 。它代表了AI从理解生命活动的产物(蛋白质),向理解生命活动指令(基因组)的又一次深刻跃进。

留下评论